تم اعتماد مجموعة اختبار SARS-CoV-2 التي طورتها شركتنا رسميًا من قبل إدارة الغذاء والدواء الأمريكية (EUA) في 22 مايوnd، حسبما أعلن الموقع الرسمي لإدارة الغذاء والدواء الأمريكية.وهذا يعني أن منتجنا قد حصل على "موافقة" في السوق الأمريكية ويمكن طرحه للاختبار على نطاق واسع في مختبرات CLIA لإصدار الشهادات الطبية في جميع أنحاء الولايات المتحدة.

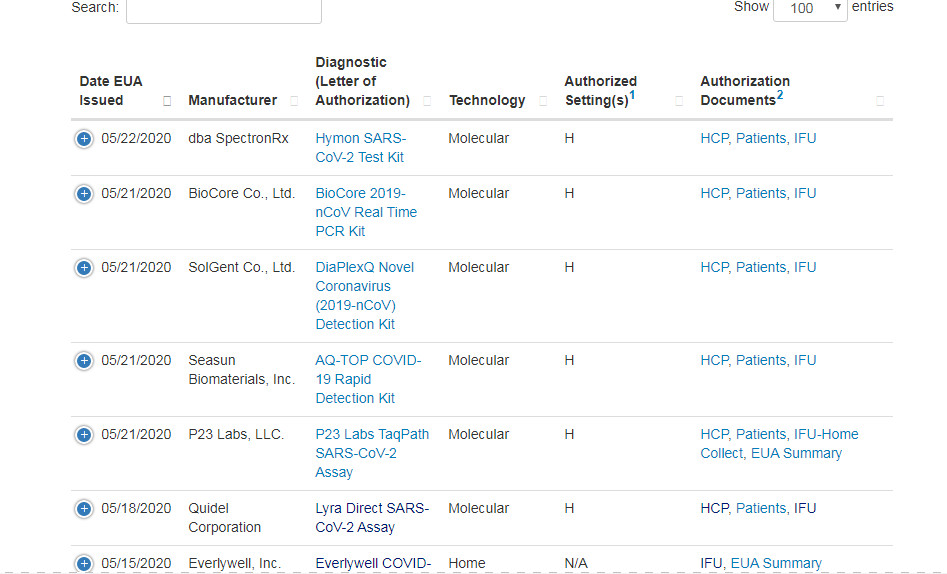
نحن أول شركة صينية تحصل على شهادة FDA EUA في الشهر الماضي، والمؤسسة الخامسة في الصين التي حصلت على US FDA EUA، والمؤسسة الوحيدة التي ليس لديها شركات تابعة في الخارج لتتم الموافقة عليها من قبل إدارة الغذاء والدواء.
قال الرئيس التنفيذي الدكتور تامي تان: "[قبل تفشي فيروس كورونا الجديد،] لم يكن لشركتنا أي علاقات تجارية مع شركة SpectronRX للأدوية في الولايات المتحدة"."[بعد تفشي فيروس كوفيد-19 في الولايات المتحدة]، اتصلت بنا شركة SpectronRX بنشاط بعد معرفة المعلومات ذات الصلة من الإنترنت والقنوات الأخرى، حيث اتصلوا بنا وعرضوا التعاون معنا.وبعد بعض المفاوضات، سمحنا لهم بتمثيل Hymon الخاص بنا®مجموعة اختبار SARS-CoV-2، التي قمنا بتطويرها وإنتاجها في أمريكا الشمالية.
كتب جون زينر، الرئيس التنفيذي لشركة SpectronRX Pharmaceuticals، لشركتنا، “يواصل وباء كوفيد-19 اختبار وتحدي النظام الطبي الأمريكي.نحن بحاجة إلى تدابير متنوعة لمكافحة الفيروس.الهيمون®تتميز مجموعة اختبار SARS-CoV-2 بكونها سريعة وبسيطة ودقيقة.ويمكن نشره في أكثر من 7000 مختبر معتمد طبيًا من CLIA في جميع أنحاء الولايات المتحدة لإجراء اختبارات واسعة النطاق.
في المستقبل، سنتعاون مع شركة SpectronRX للأدوية لمواصلة تزويد المرضى والأطباء بقيمة فريدة في مجال تشخيص وعلاج الأمراض الرئيسية.
وقت النشر: 29 مايو 2020

